
Arkiv: Arne Holst-Jensens blogg
Blogginnlegg fra 2010. Arne Holst-Jensen, forsker, Veterinærinstituttet
Syntetisk biologi – genteknologi for morgendagen eller neste århundrede?
Denne artikkelen er over ti år gammel og kan inneholde utdatert informasjon.
Det er nå drøyt tre måneder siden J. Craig Venter og hans medarbeidere presenterte det første eksemplet på en levende organisme med et syntetisk arvestoff (Gibson m.fl. 2010). Er syntetisk biologi ren science-fiction eller vil konsekvensene berøre oss allerede i nær fremtid?
I mitt forrige blogginnlegg skrev jeg om bio-hackere og biologiske byggeklosser. Syntetisk biologi er den ytterste variant av dette.
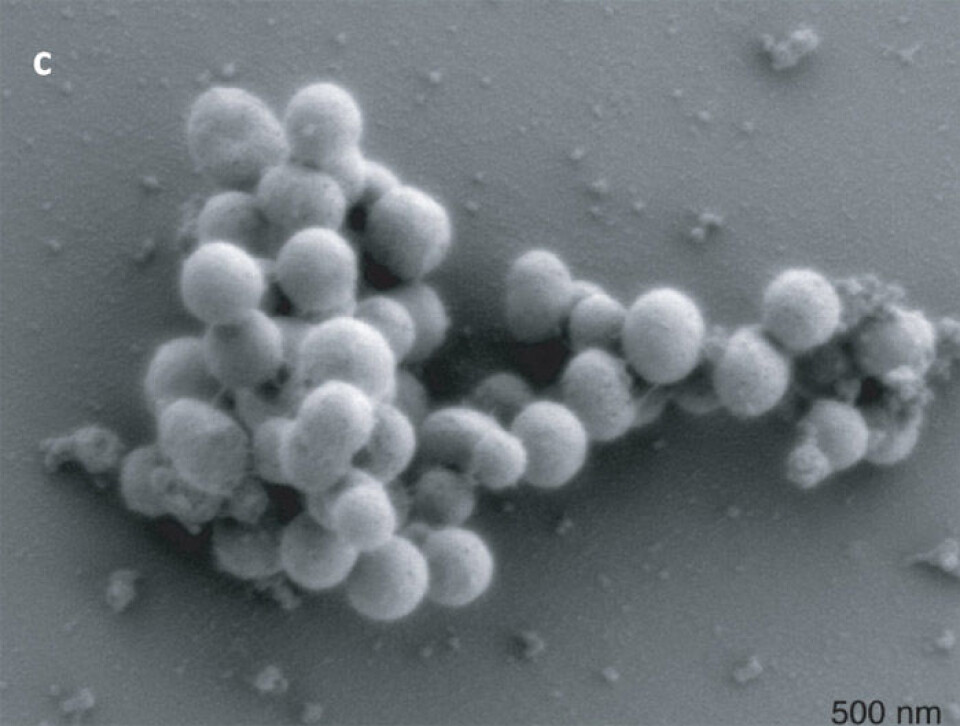
Livsformen Venter og hans medarbeidere har skapt er nærmest en kopi av en eksisterende livsform. Det forskerne gjorde var å fjerne alt arvestoffet i en bakteriecelle og erstatte det med en kjemisk fremstilt kopi av arvestoffet til en nærtstående art, og deretter få cellen til å leve videre og dele seg.
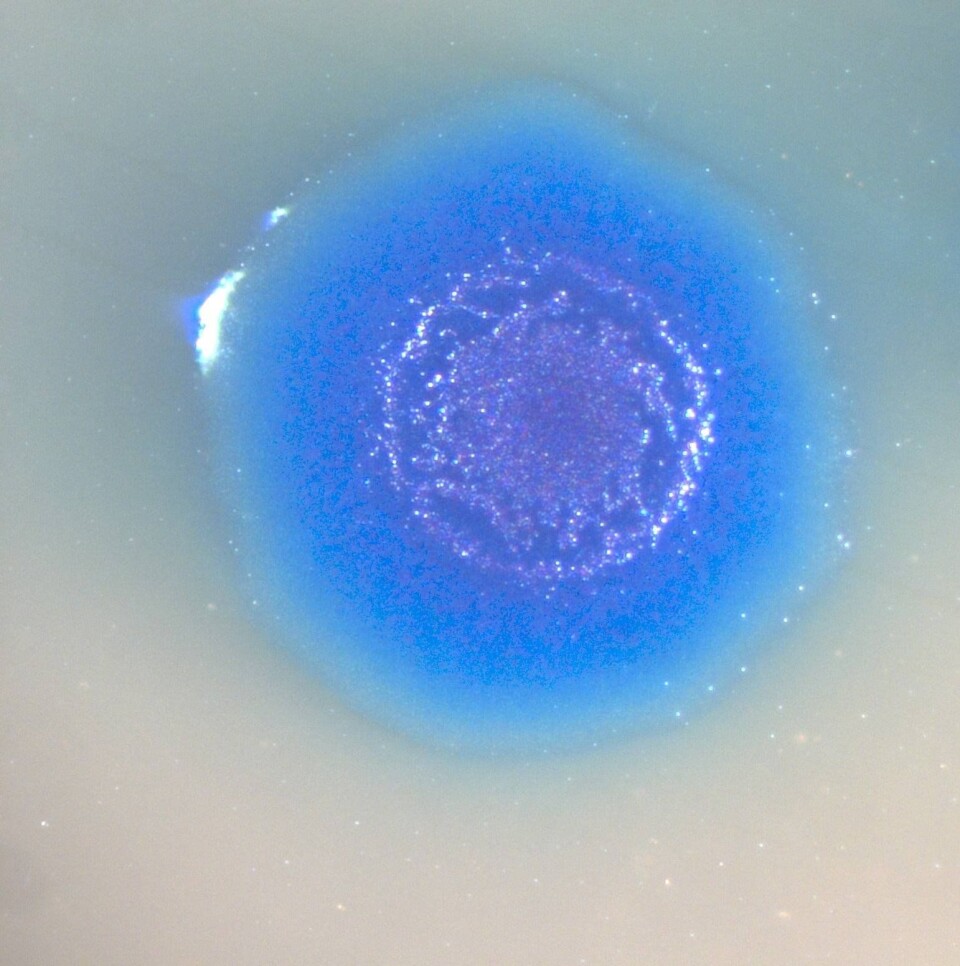
Det syntetiske arvestoffet var endret litt for å tilføre noen få nye egenskaper. Blant annet blir cellene blå til forskjell fra hvite normalceller, og det er tilført minst ett gen som gjør cellene i stand til å vokse på vekstmedier hvor normale celler ville dødd. Gjennombruddet som ble presentert i mai i år bidro til at mange flere innen vitenskapsmiljøene tror på at helt nye livsformer kan skapes i laboratorier.
Det blir kanskje lettere å visualisere det gjennomførte eksperimentet om man ser for seg en menneskecelle hvor man erstatter arvestoffet med arvestoff fra en menneskeape og deretter får den til å vokse opp til et helt vesen. Har den i tillegg fått gener for å bli blå og overleve i en skadelig atmosfære så har man på det nærmeste en Avatar slik de fremstår i filmen av samme navn. Vær likevel klar over at det er meget store fundamentale forskjeller på å gjøre dette med bakterier sammenlignet med dyr eller planter.
I årene som kommer vil Venter og hans medarbeidere med stor sannsynlighet lykkes med å utvikle livsformer som avviker betydelig fra alle kjente livsformer. Tusenvis av gener kan være fjernet og et titalls eller mer kan være tilført. Slike nye livsformer vil neppe kunne krysse seg med sine opprinnelige former, og faller derfor utenfor de klassiske oppfatningene av arter.

Utgangspunktet vil uansett være relativt primitive livsformer, som bakterier og bakterielignende organismer. Men misforstå meg rett, - også disse livsformene er svært kompliserte.
Arvestoffet er organisert i kromosomer. Bakterier har bare ett kromosom, mens dyr og planter har flere kromosompar. Mennesket har for eksempel 23 par kromosomer. Å erstatte et helt kromosom er meget vanskelig, men kan på mange måter sammenlignes med det Venter og hans medarbeidere utførte på bakterien. Det er derfor ikke urealistisk å tenke seg at denne teknologien vil gjøre det mulig å bytte ut et kromosompar i en plante eller et dyr og erstatte det med et kunstig kromosompar der man har satt inn gener som koder for en pakke av nye egenskaper.
Teknikkene som benyttes til genmodifisering i dag gir ingen mulighet for å bestemme på forhånd hvor nye gensekvenser blir satt inn i eksisterende kromosomer. Som regel vil det også oppstå små utilsiktede endringer andre steder i arvestoffet, og noen av disse kan være vanskelige å oppdage. Da blir det også vanskelig å forutsi effekten disse endringene har.
Om man kan erstatte hele kromosomer kan det i hvert fall teoretisk redusere risikoen for at utilsiktede endringer i arvestoffet finner sted. Venter og hans medarbeidere viste at det lar seg gjøre å syntetisere kromosomer, slik at man kjenner hele baserekkefølgen. Plassering av nye gener blir dermed langt lettere å kontrollere.
I mais arbeides det allerede med et system for å sette inn et kunstig kromosom med pakker av nye gener. Dette systemet bygger imidlertid på et slags ekstrakromosom som finnes naturlig i noen typer av mais (Birchler m.fl. 2008).
Det er klart at vi står overfor mange nye, viktige og vanskelige problemstillinger. Det er utvilsomt lenge til vi forstår alle muligheter og konsekvenser av den teknologiske utviklingen. Vil for eksempel endringer på et kromosom påvirke andre kromosomer? Vi vet med sikkerhet at gener påvirker uttrykket av hverandre, også på tvers av kromosomer. Så risikovurdering av organismer med halv- eller helsyntetiske kromosomer blir utfordrende. Sammenlignet med mange av dagens foredlingsteknikker, også innenfor tradisjonelt landbruk (uten genmodifisering), vil de nye teknologiene både ha fordeler og ulemper i forhold til helse-, miljø- og samfunnsrisiko.
Jeg forstår hvis du som leser dette blir bekymret. Men spørsmål om risiko kommer opp så ofte at vi i praksis aldri får reflektert over mulighetene. Både myndigheter, vitenskapelige eksperter, organisasjoner og legfolk bidrar aktivt til høringsprosesser rundt regelverk og risikovurderinger bl.a. av genteknologi og GMOer. Det vil også være tilfelle i fremtiden. Jeg er derfor trygg på at all risiko vil bli tatt på alvor og at ingen nye produkter vil bli tillatt uten at de er grundig risikovurdert og funnet trygge. Venter og hans medarbeidere har lenge vært pådrivere for diskusjoner omkring etikk, muligheter og betenkeligheter ved genteknologi, men klarer å ha flere tanker i hodet samtidig.
Derfor vil jeg for en gangs skyld oppfordre til å la bekymringene ligge litt og spørre deg om du kan se noen muligheter som kan bidra til for eksempel å løse store globale utfordringer som klimaendringer, sult og sykdom? Å overlate alle fremtidens muligheter til private amerikanske initiativer kan føre til at vi får mer fokus på fortjeneste enn på fellesskapets interesser og behov. Og endelige blir det kanskje ikke så mange norske arbeidsplasser av det heller.
Referanser:
• Birchler J, Yu W, Han F. Plant engineered minichromosomes and artificial chromosome platforms. Cytogenetics and Genome Research, 2008; 120:228–232.
• Gibson, DG m.fl. 2010. Creation of a bacterial cell controlled by a chemically synthesized genome. Sciencexpress, 20 May 2010:1-7






