
Screening: Genial forebygging eller sykeliggjøring av friske personer?
For mange sykdommer er overlevelsen dårlige for pasienter med langtkommen sykdom. For å bedre overlevelsen, har masseundersøkelser i form av screening for tidligere diagnose blitt vanlig. Noen former for screening er lite omstridt, mens andre er hyppig diskutert. Er screening effektiv forebygging eller sykeliggjøring av friske kvinner og menn?
Venninner av Anna har i flere år gått til privat mammografi (røntgen) undersøkelser for å avdekke mulig brystkreft. Flere har mast på at Anna også skal la seg undersøke.
Screening kan både sees på som en genial tidlig diagnose hvor sykdommen behandles før den blir alvorlig, og en sykeliggjøring av ‘friske’ personer
Ved 50 års alder dumper det ned en invitasjon til det offentlige Mammografiprogrammet.
Anna blir forvirret – Hvorfor ble hun ikke invitert før? Hvorfor skal hun gå nå?
Vi møter mange ulike former for screening i dagens samfunn, både for kreft, hjertekarsykdom og medfødte lidelser hos spedbarn. Mens pasienter normalt kommer til sykehuset for behandling av langtkommen sykdom, snur screening alt på hodet med innkalling av øyensynlig «friske» personer. På vegne av Forskingsrådet evaluerte vi i 2014 det norske Mammografiprogrammet for tidlig diagnose av brystkreft. Blant friske kvinner som møter til programmet anslo vi at drøye 1/3 av fremtidige brystkreftdødsfall forebygges med screening (1). Dette er gode nyheter, men screening er ikke uproblematisk. For hver kvinne som får forlenget livet takket være screeningen, anslo vi at 368 kvinner må inviteres 10 ganger til screening. I praksis reddes én kvinne, mens mange andre setter av tid til undersøkelser og risikere falske positive funn. Aller mest alvorlig er overdiagnostikk, funn og behandling av krefttilfeller man kunne levd lykkelig uvitende om hvis det ikke var for screeningen (2).
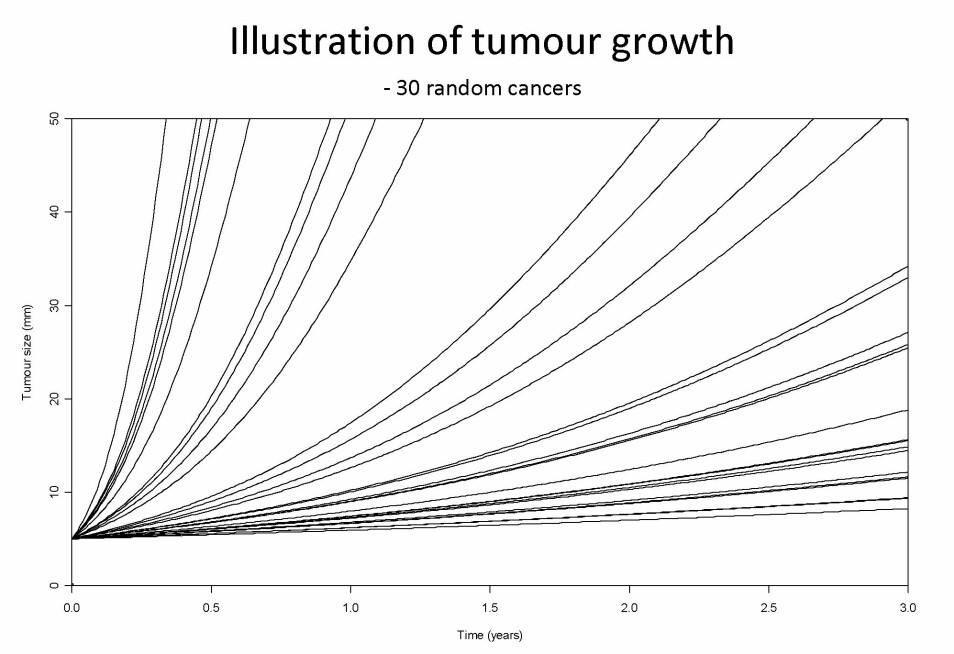
Problemet er at kreft utvikler seg svært ulikt (3), ingen vet hvordan en svulst vil utvikle seg, eller når pasienten vil dø av andre årsaker. Mens noen kreftsvulster er viktig å behandle, vil andre utvikle seg så sakte at pasienten dør av andre årsaker lenge før kreften gir symptomer. I praksis er screening litt som forsikring – mange bidrar med litt for å hindre at noen dør fra oss så altfor tidlig. Har screening positiv effekt? Dette må vurderes for hver sykdom og hver enkelt test. Screening kan både sees på som en genial tidlig diagnose hvor sykdommen behandles før den blir alvorlig, og en sykeliggjøring av «friske» personer.
Hvorfor forsker vi på screening?
Ved Oslo Universitetssykehus jobber vi med å utvikle nye statistiske modeller for å beregne graden av overdiagnostikk i screeningprogrammer mer presist. I dag avsluttes det norske Mammografiprogrammet ved 69 års alder, men er det fornuftig å screene lengre når kvinnene lever lengre? Når man skal vurdere øvre alder for screeningprogrammer, er graden av overdiagnostikk avgjørende.
I Norge har vi i dag offentlige screening-programmer for bryst- og livmorhalskreft, og prøver ut screening for tarmkreft. PSA test for tidlig diagnose av prostatakreft er derimot ikke vurdert som fornuftig screening i Norge
På den ene siden ønsker å hindre brystkreftdødsfall, på den andre siden unngå unødig behandling. Vi ønsker at bestemoren ikke dør fra barnebarna, men også at hun får et godt liv og tid til nettopp barnebarna. Screener vi en 98 år gamle kvinne for å finne kreft som kanskje først kunne tatt liv om 8 år, gjør vi i praksis mer skade enn nytte da svært få lever til de er 105 år. Å forstå konsekvenser av ulike screeningvalg er ikke lett, og som del av «CISNET - Cancer Intervention and Surveillance Modeling Network» (4) jobber vi med ledende forskingsmiljøer ved blant annet Harvard Universitet (Boston, USA), Stanford Universitet (Palo Alto, USA) og Erasmus Universitet (Rotterdam, Nederland).
Blant unge kvinner under 50 år er brystkreftsvulster vanskeligere å se på screening og man får flere falske positive funn, men hvor stort er dette problemet i forhold til gevinsten av screening? Avanserte simuleringsmodeller gir oss en ide om fordeler og ulemper ved ulike screeningstrategier, som igjen kan brukes for utarbeidelsen av gode anbefalinger.
Suksesshistorier og historiske feiltrinn
Screening etter forstadier av livmorhalskreft er lite omstridt. Man har negative sider ved screeningen, men den redder også svært mange kvinner fra en tidlig død (5). De siste tiårene har livmorhalskreft gått fra en vanlig til uvanlig dødsårsak i land med screeningprogrammer. Mer omstridt er PSA testene for tidlig diagnose av prostatakreft blant menn. Prostatakreft vokser svært sakte og behandling har store bivirkninger. Spørsmålet er om PSA-screening gjør mer skade enn nytte. Studier tyder på at rundt 1 av 3 menn i 70-årene har tidlige tegn til prostatakreft (6). Ønsker vi at nesten 1/3 menn skal behandles for en sykdom de kunne dø lykkelig uvitende om? En norsk evaluering endte med ikke å anbefale PSA screening i Norge (7).
I praksis må enhver screening vurderes nøye før man lager generelle anbefalinger. I Sør-Korea ble screening for skjoldbruskkjertelkreft vanlig på 1990-tallet. Det kunne lenge se ut som en utrolig suksesshistorie. Stadig flere menn og kvinner «pustet lettet ut» når screeningen «reddet» livet deres, men en sjelden sykdom som tok få liv ble snart en folkesykdom (8). Det ble åpenbart at de fleste aldri ville fått kreftdiagnosen uten screening, og man la raskt om. Når vi nå innfører tarmkreftscreening i Norge bygger vi på internasjonale studier og tester ut ulike metoder i Norge før landsdekkende screening innføres, nettopp for å sikre at screeningen gir større nytte en skade (9).
Bør jeg gå til screening?
I bunn og grunn vil screening alltid være et individuelt valg, men god kunnskap er avgjørende for gode beslutninger. Noen vil være ekstra redde for unødig behandling, mens andre vil ofre svært mye for å redusere muligheten for å dø av kreft. For mange er de offentlige anbefalingene fra fagmiljøene et godt utgangspunkt.
I Norge har vi i dag offentlige screeningprogrammer for bryst- og livmorhalskreft, og prøver ut screening for tarmkreft. PSA test for tidlig diagnose av prostatakreft er derimot ikke vurdert som fornuftig screening i Norge.







